一、基本原理
在超声成像扫描阶段,换能器发射声波脉冲到人体的感兴趣区域中。然后,后向散射回波信号被采集并经过信号后处理生成超声图像。图1所示为超声成像的基本原理。在进行超声成像时,如图 (a)所示,首先通过对能够产生和检测超声波能量的压电换能器进行电激励发射超声波束对成像介质进行扫描。然后,如图 (b)所示,发射的超声脉冲在介质中进行传播并与介质中的散射点相互作用。由于介质的不均匀性以及和超声脉冲之间的相互作用,产生的反射和散射回波将会增加。最后,如图 (c)所示,这些回波向后传播到切换为接收模式的换能器阵列上,并被转换成电信号(即原始通道数据)。这些回波包含了成像介质的重要特性,通过对接收到的信号进行相应的后处理,重建得到待成像介质的超声图像。
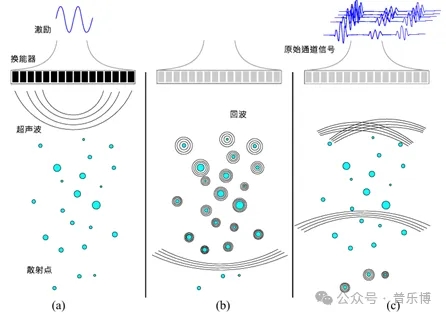
图 超声成像基本原理
二、基本结构
无论是柔性还是刚性探头,在结构上均大致分解为声透镜、匹配层(一层或多层)、压电材料(如锆钛酸铅)、上下电极层(如Au或铂Pt)、背衬及封装壳体等。压电换能器是一种叠堆层式结构,因此任意一层的设计和制备需要根据使用场景不同进行特殊设计。

图超声换能器基本结构(a)结构爆炸图和关键组件;(b)传统刚性探头和复合柔性超声贴片乳腺检查扫描方式与 贴片超声对应乳房乳腺密度区域
1.压电元件 压电元件是超声换能器的核心功能单元,通常采用锆钛酸铅(PZT)压电陶瓷多晶材料制成。其制作过程包括高温高压极化赋予压电特性,再根据目标频率切割成特定厚度的薄片,并在上下表面镀覆电极。阵元在结构上呈长方体:厚度直接决定换能器的中心频率;长度方向(垂直于阵列排列方向)的尺寸(通常为6–13 mm)主要用于调节灵敏度与波束聚焦,其谐振频率远低于工作频段;宽度方向则与阵元间距(pitch)相关。为抑制宽度方向谐振对厚度振动的干扰,每个阵元常沿宽度方向再分割为若干微元,各微元间电极并联、协同工作,从而获得更单一的振动模态。
2. 背衬层 背衬层附着于压电元件背面,主要起阻尼与吸声作用。其设计需兼顾两方面:一是通过增加机械阻尼促使压电元件在激励后迅速停止振动,从而缩短脉冲长度、提升轴向分辨力;二是吸收并衰减向后传播的超声波,减少界面反射造成的信号干扰。背衬材料的声阻抗匹配程度直接影响换能器性能:若与压电元件声阻抗接近,则向后波几乎无反射进入背衬并被吸收,可获得干净短脉冲,但会降低换能器灵敏度;若阻抗差异显著,则较多能量被反射回压电片,灵敏度提高,但脉冲持续时间延长。实际设计常在脉冲宽度与灵敏度之间寻求折衷。
3. 匹配层 由于压电陶瓷(声阻抗约33 Mrayls)与人体软组织(约1.5 Mrayls)之间声阻抗差异巨大,直接在界面处会产生强烈反射,导致超声能量难以进入人体。为此,在压电元件前方添加一至多层匹配层,起阻抗过渡作用。匹配层需满足低超声衰减、厚度为四分之一波长的奇数倍(通常取λ/4),以及特定声阻抗值等要求。多层匹配能拓宽频带并提高传递效率,但工艺难度相应增加,故实用中多采用双层结构。随着频率升高,波长变短,匹配层厚度显著减小(例如10 MHz对应约0.05 mm),制作精度要求更高。
4. 声透镜 声透镜主要用于在垂直于阵列排列的方向上对声束进行几何聚焦,其原理是利用声波在不同声速介质界面发生的折射使波束会聚。通常选用声速低于人体组织的材料制成凸柱面透镜,通过计算曲率半径可设定固定的聚焦深度。另一种方式是将压电元件本身制成凹曲面,从而在该方向上实现直接聚焦,此时探头表面可为平面。声透镜作为接触人体的最外层,需采用生物相容性好、耐磨性强的材料,日常维护应保持其表面清洁,避免耦合剂残留影响声学性能。
三、主要类型
1.机械扇(形)扫(描)探头
机械扇扫探头通过电机驱动单元式换能器进行机械摆动或旋转,实现声束的扇形扫描。早期曾广泛用于腹部和心脏检查,现已几乎仅限于眼科A/B超应用。其外形通常呈圆柱形手柄配半球形端部,接触面两侧常切出浅平台以指示扫描方向;工作时因存在机械运动,可感知振动与噪声。探头端部为透声塑料制成的充油腔体,内置一至三个单元式换电陶瓷换能器,由柄内电机驱动摆动或轮流旋转工作,从而采集回波并生成扇形图像。该图像在近场中心存在无信号的“缺损”区域,即缺少“扇轴”部分。此外,曾出现一种高档的环阵变型,其晶片被切割为同心圆环并按阵列方式工作以实现多点聚焦,但因制造复杂、成本高昂且逐渐被电子扫描探头取代,现已少见。
2. 平面线阵探头


图 线阵探头,其成像为矩形
平面线阵探头采用数十至数百个独立阵元沿长边方向线性排列,通过电子切换与组合实现声束的平移扫描。在凸阵探头普及前,它是腹部检查的主力(频率约3.5 MHz),此后主要转向小器官及表浅组织检查,频率多升至5 MHz以上甚至9 MHz。探头外形多为长方形,长边对应晶片排列方向;结构从外至内依次为声透镜、双层匹配层、切割成窄条状的压电晶片阵元(阵元间填充吸声橡胶)、背衬以及前置放大电路。工作时通常以约十个阵元为一组发射与接收,通过递推组合与电子开关切换,形成沿长边方向的扫描声束,最终合成矩形图像。在一维探头中,晶片短边方向不作切割;而在1.25、1.5、1.75维探头中,短边方向也进行切割并引入电子聚焦,以改善该方向的声束性能。
3. 凸阵探头
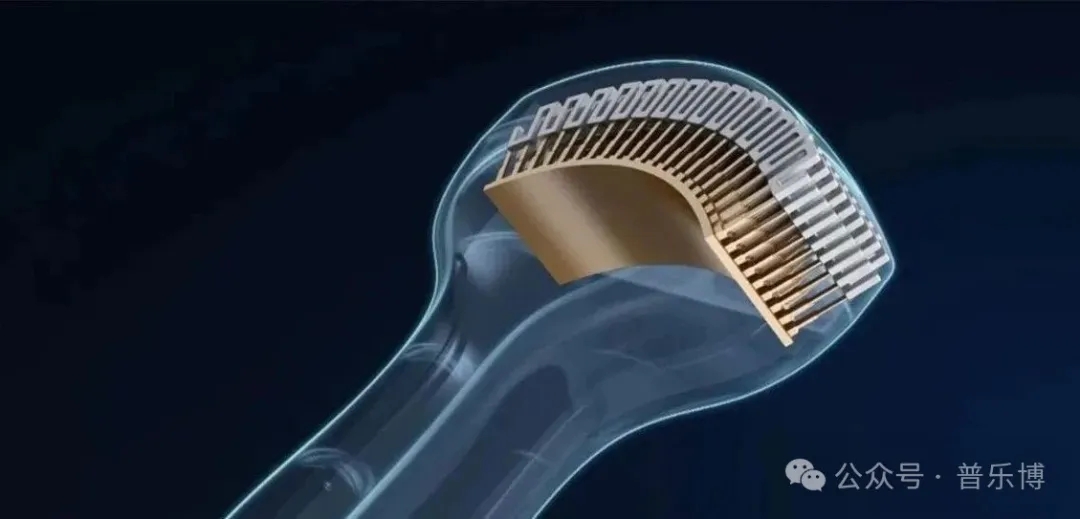
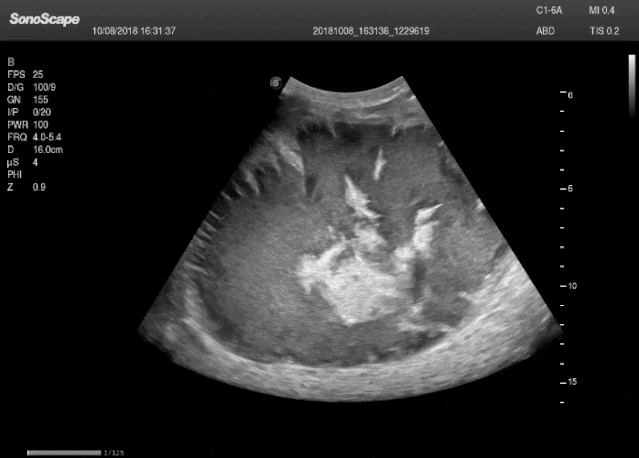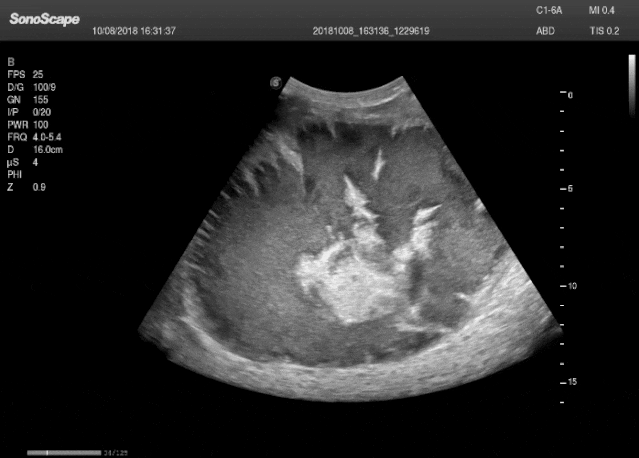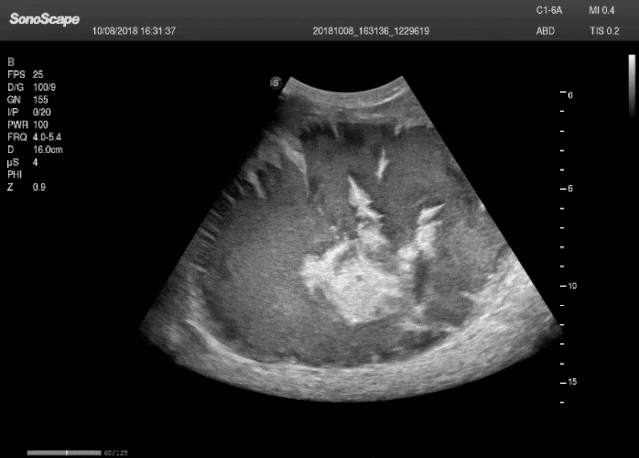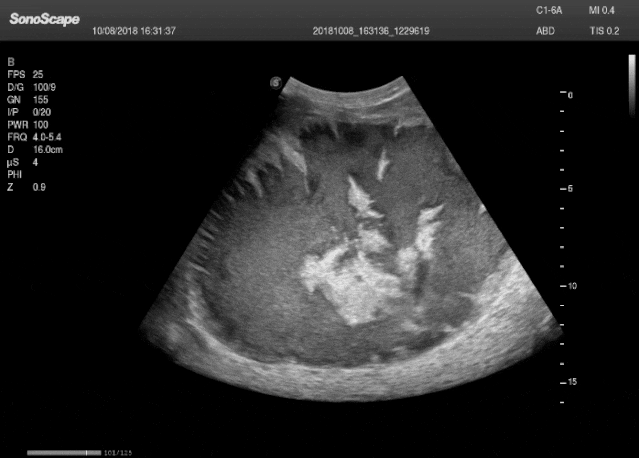
图 凸阵探头,其成像为扇形
凸阵探头可视为将线阵探头的平面晶片改为弧形排列,其声束通过类似线阵的电子扫描方式工作,但因阵元呈弧形分布,扫描图像呈现扇形,从而扩大了中远场的视野范围。依据晶片曲率半径(R)的不同,其用途有所区分:R大于30 mm者主要用于腹部检查;小R(10–20 mm,常称“微凸”)则适用于心脏检查。探头外形特点是辐射面为向外凸出的弧形,内部结构从声透镜、匹配层、压电晶片到背衬均与线阵探头相似,仅晶片形状改为弧形。所生成的扇形图像完整连续,即“只有扇面,无扇骨部分”,与机械扇扫的中心缺损形成区别。
4. 相控阵探头
相控阵探头采用电子延迟技术同时实现声束的聚焦与偏转,从而无需机械运动即可获得扇形扫描,故亦称电子扇扫探头。其主要用途是心血管的彩色血流成像,通常在同一探头上通过切换工作模式,分别获取黑白解剖图像、彩色血流图像及多普勒频谱。探头外形接近正方形,类似辐射面较小的平面线阵;内部结构与线阵相似,包含声透镜、匹配层、压电阵元及背衬等。其核心特点在于采用两组延迟线:一组用于多段电子聚焦,另一组专司声束方向偏转,使所有阵元可协同工作实现扇形扫描。在连续波多普勒模式下,半数阵元并联发射、另半数并联接收。最终生成的扇形图像完整无缺损,且具有较好的近场视野,适用于经肋间等声窗受限的心脏检查。

表 各类探头的特性
四、超声机器人技术
超声机器人技术正以前沿的智能化与精准化变革,深度融入现代医疗的核心场景。通过融合人工智能与自适应控制系统,它不仅实现了扫描路径的自主优化与实时参数调节,更在肿瘤消融、神经调控等复杂治疗中展现出高精度引导能力。随着多模态影像融合与5G远程协作的突破,超声机器人已跨越空间限制,赋能远程诊断、急救现场与家庭健康管理。当前,该领域持续向全流程智能化、操作精准化与平台集成化演进,不断拓展其在疾病筛查、手术导航及个性化治疗中的全新应用形态。以下将结合最新研究,进一步解析超声机器人的关键技术进展与未来发展方向。
1.肺部超声成像引导机器人技术
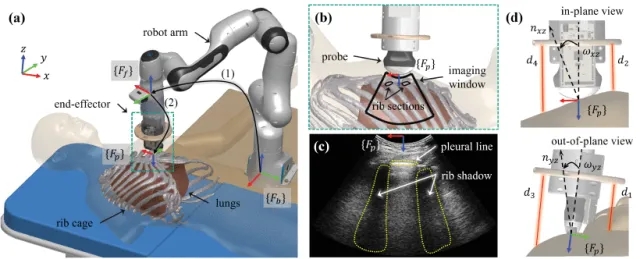
图 基于机器人超声检查(Robotic Ultrasound System, RUSS)的LUS场景:(a) RUSS的设置和坐标约定。(b) 超声探头的放置位置以获取纵向肋间视图,即LUS的SIP。(c) 从SIP获取的代表性超声图像。(d) 探头的平面内视图和平面外视图。红色光束代表光学传感器的距离测量。
美国伍斯特理工学院 Haichong K. Zhang团队提出了一套用于机器人肺部超声检查的标准成像平面(SIP)自主导航框架。该系统基于实时超声图像反馈,能够从初始粗略定位(误差范围1-2厘米)出发,完成“最后一厘米”的高精度探头引导。通过集成定制设计的主动终端执行器(A-SEE)并结合基于图像的视觉伺服控制(IBVS)算法,实现探头位姿的自主实时调整,从而保障成像的一致性与高质量。
研究在模拟肺模型及五名男性志愿者中对该系统进行了验证。实验结果表明,系统可在平均5秒内成功导航至目标SIP,探头定位误差小于2毫米,旋转误差小于2度。此外,系统在面对个体解剖结构差异时仍表现稳定,体现出良好的跨患者适应性,有助于实现标准化的诊断操作。
本工作验证了该导航框架的高精度与临床可行性,为肺部超声的自动化、标准化检查提供了可靠方案。该框架具备良好的扩展性,未来可进一步推广至肝脏、甲状腺等其它器官的超声检查任务中,并在更广泛的人群中验证其普适性与有效性。
2. 人工智能技术结合机器人引领自动化手术新方向
慕尼黑工业大学计算机辅助医疗与增强现实团队CAMP(Computer Aided Medical Procedures & Augmented Reality)在其综述中指出,随着人工智能与传感技术的快速发展,自动化医疗机器人已在医疗领域获得广泛关注。其中,机器人超声系统(RUSS)因其独特的优势,受到了学界与业界的共同重视。与多数手术机器人不同,超声检查具备非侵入性特点,这使其在伦理、法律及监管层面面临的约束相对较少。同时,超声成像凭借其便携、实时、无辐射等优势,已成为基层医疗中不可或缺的工具。
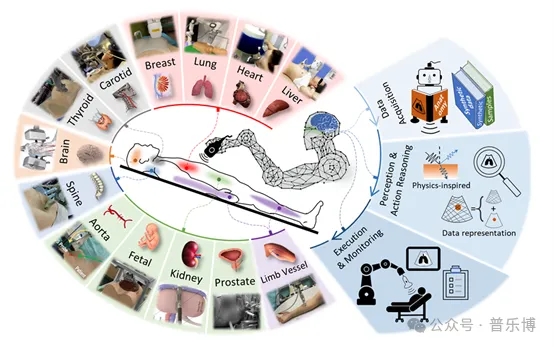
左图:机器人超声成像在临床上的典型应用。从2点钟方向开始逆时针依次为:肝脏、心脏、肺、乳房、颈动脉、甲状腺、大脑、脊柱、主动脉、胎儿、肾脏、前列腺、四肢血管。右图:为了自主操控超声探头以获得诊断视图,设想中的智能机器人超声医生应能够利用先前的解剖学知识并分析实时观察结果来进行行动推理。
3. 穿刺机器人技术新突破:更精准的经皮监测系统
在超声引导的经皮针刺穿刺临床实践中,针体在组织内行进时常因复杂的相互作用而偏离超声成像平面,导致术中实时监测困难。为解决这一关键挑战,慕尼黑工业大学CAMP团队在其最新研究中提出了一套机器人辅助超声成像系统。该系统能在针体脱离成像平面时,自动调整探头位姿以恢复针体的实时可视性。
研究采用了一种具有对抗性结构的网络模型,该模型能够生成在高层特征空间中与真实标注高度一致的分割掩模。团队系统探究了多种训练损失函数及其组合对分割效果的影响。当系统检测到探头与针体之间的位置失配时,机器人会自主启动横向搜索机制,通过优化位置与旋转调整,重新获取针体的清晰图像。
在离体猪组织实验中,该方法实现了对经皮针的精准分割,其尖端定位误差为0.37±0.29毫米,角度误差为1.19±0.29°。此外,在全部45次试验中,系统均成功恢复了针体在超声图像中的可视性,重新定位误差控制在1.51±0.95毫米和1.25±0.79°以内,验证了该方法的有效性与可靠性。
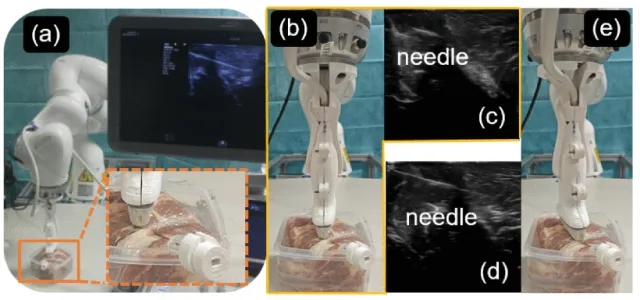
图 针插入离体猪样本的示意图 (a) 是整体场景,(b) 和 (e) 分别表示失配情况和期望情况。(c) 和 (d) 分别是在 (b) 和 (e) 情况下获得的相应B模式图像。
4. 结合虚拟现实技术的并行计算超声手术机器人实现复杂手术
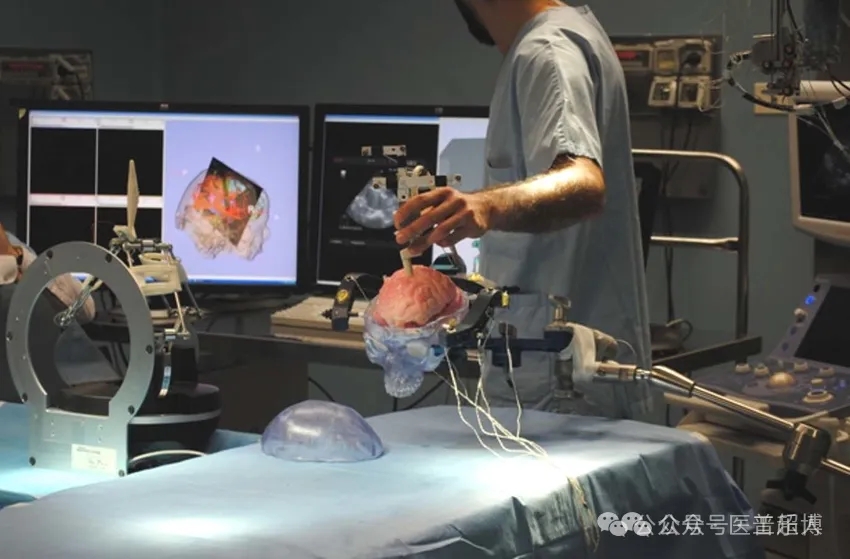
图 在意大利维罗纳的Ospedale Maggiore医院举行的ROBOCAST项目最终演示中展示了术中超声导航机器人:使用光学跟踪的US探测器,可以在三维场景中实现图像平面的可视化
中国科学院Fei-Yue Wang团队在研究中指出,自20世纪90年代末起,欧美及日本学界对自动化超声系统的研究兴趣持续增长,其核心目标是解决临床实践中手持探头难以长时间保持精准定位等问题。
该研究强调,机器人术中超声系统的创新应用,关键在于虚拟环境与并行系统的协同,以此提升诊断成像的精确性与效率。通过自动化与先进控制系统,机器人超声旨在优化超声引导手术流程,减少人为误差。研究进一步探讨了机器人技术在经直肠超声(TRUS)及经食管超声心动图(TEE)等具体场景的应用潜力。例如,TEE机器人系统可显著减轻操作者的体力负荷,简化流程,从而提升手术效率。
此外,研究团队介绍了一种新型虚拟平台。该平台利用3D建模与超声成像模拟技术,使医生能够在术前进行手术预演与路径规划,有效提高了手术的安全性及成功率。文中的多项案例研究初步展示了该集成系统在临床中的实际效果与潜在优势。

图 使用混合整数遗传算法(GA)进行自动视图优化的结果,优化了(a)双腔静脉视图,其中基准点位于下腔静脉(IVC)、上腔静脉(SVC)和右心房(RA)中心,以及(b)ME主动脉瓣松弛视图,基准点位于主动脉瓣和二尖瓣中心。上方行显示了遗传算法优化过程中惩罚值的变化,以及随着代数增长最终达到的收敛情况。
5.深度与热成像融合技术的全自动化超声机器人取得新进展
超声检查的准确性与效率高度依赖操作者经验,这不仅限制了其应用的一致性与普适性,也导致超声技师因重复性操作而面临肌肉骨骼劳损等职业健康问题。为应对这些挑战,融合机器人技术的自动化超声系统逐渐成为研究热点,但现有系统在扫描区域定位与探头操控等方面仍需较多人工干预。
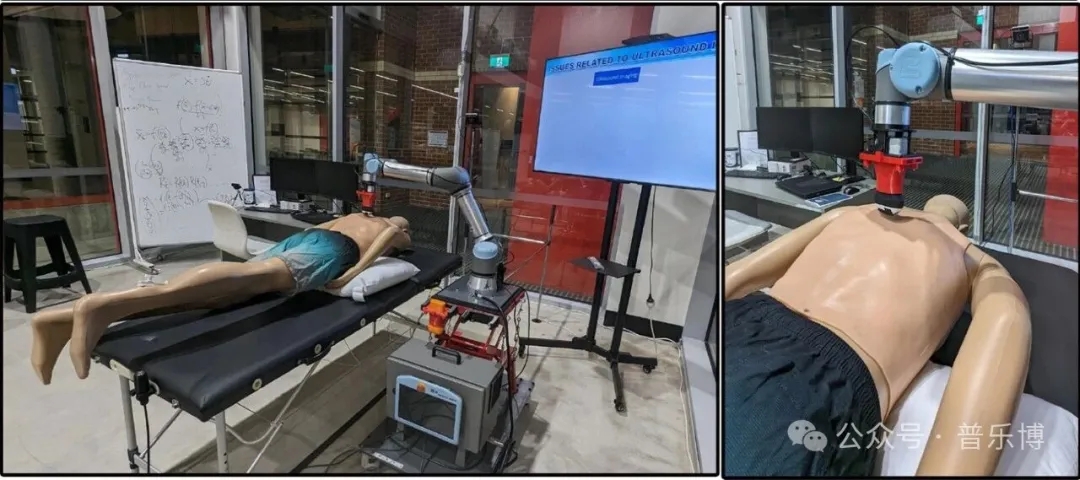
图 机器人超声成像系统的不同视角
实验从多角度验证了系统性能:在扫描区域定位方面,模板匹配算法表现出良好的重复性与稳定性;探头操控方面,力矩反馈控制能有效维持探头与体表的垂直姿态;志愿者实验进一步证明,该系统可成功完成腰部超声成像,在图像采集的准确性与一致性上优于手动操作,展现出良好的临床应用潜力。
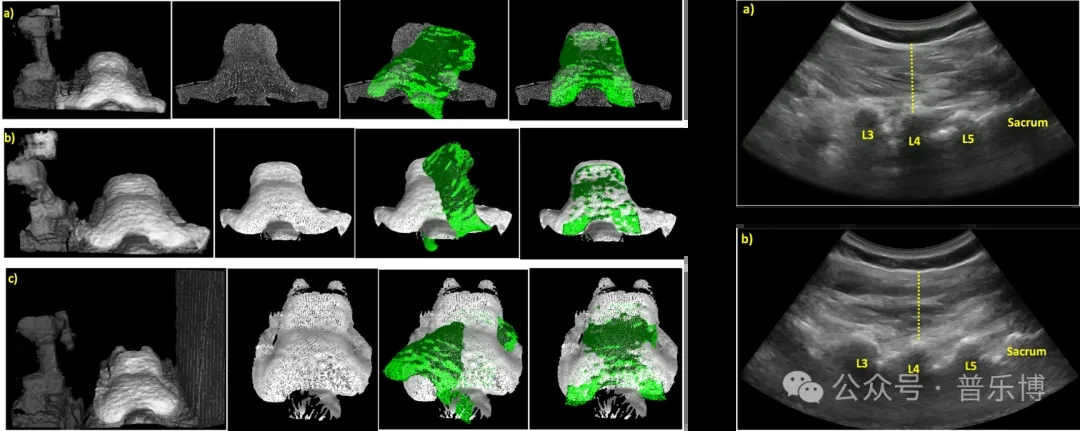
左图:针对三个不同个体(a–c)的模板匹配算法,显示原始数据、预处理点云、FGR后对齐的模板和ICP后对齐的模板。右图:志愿者实验,(a)自主成像方法,(b)手动成像方法。两张图均显示了显著的腰椎L3、L4、L5和骶骨,并用线条表示多裂肌的厚度。

Copyright © 2018,All rights reserved 广州辰方互联信息科技有限公司 版权所有 备案号:粤ICP备18085845号
联系电话:020-37681030
销售热线:18520175978(微信同号)
公司地址: 广州市海珠区红卫新村西街29号UP智谷B1栋417室
